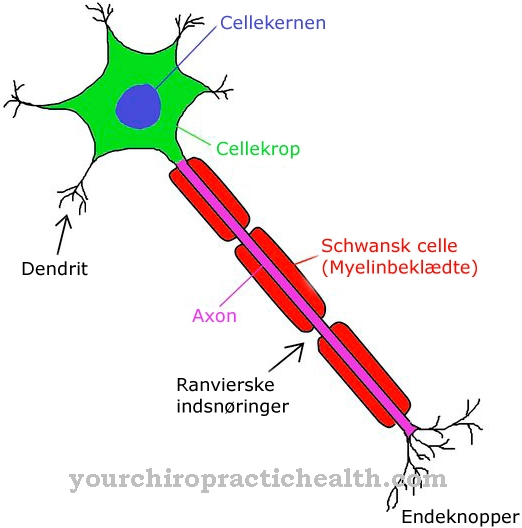
fluor reprezentuje pierwiastek o liczbie atomowej 9 i należy do halogenów. Jest to silnie korozyjny gaz, który powoduje poważne uszkodzenia błon śluzowych. Fluor jest stosowany w medycynie w postaci soli, fluoru, do wzmacniania zębów.
Co to jest fluor?
Fluor jest silnie żrącym i reaktywnym gazem, nie jest związkiem, ale pierwiastkiem chemicznym należącym do halogenów. Z liczbą atomową 9 jest najlżejszym halogenem. W naturze fluor występuje głównie w postaci soli - fluorków.
Gazowy fluor jest mało stabilny i reaguje z prawie wszystkimi związkami i pierwiastkami bezpośrednio po jego wytworzeniu. Tylko w przypadku gazów szlachetnych, helu i neonu, nie ma reakcji. Tę niezwykle silną reaktywność można wytłumaczyć bardzo silnym powinowactwem do elektronów. Zawsze odbiera elektrony swoim partnerom reakcji i dlatego jest najsilniejszym utleniaczem. Nazwa fluor pochodzi od łacińskiego słowa „fluores” (rzeka). Jako fluorek wapnia (fluoryt) służy jako topnik do rud.
Dodanie fluorytu do rud obniża ich temperaturę topnienia, dzięki czemu szybciej stają się płynne. Z koncepcyjnego punktu widzenia w medycynie istnieje termin fluoru narządów płciowych określający bezkrwawe wydzielanie wydzieliny z żeńskich narządów płciowych. Jednak fluoru narządów płciowych nie należy mylić z pierwiastkiem fluoru.
Funkcja, efekt i zadania
Fluor nazywany jest niezbędnym pierwiastkiem śladowym. Jednak znaczenie fluoru jest kontrowersyjne. Wiadomo, że fluorki mają właściwości ochronne przed zębami. Fluor może wzmacniać zęby i jednocześnie hamować niektóre enzymy bakterii próchnicy, które powodują rozpad węglowodanów.
Fluorki działają bezpośrednio na ząb. Doustne spożycie fluoru nie ma wpływu na zęby. Zęby składają się głównie z mineralnego hydroksyapatytu. Hydroksyapatyt może zostać zaatakowany przez kwasy powstające w wyniku rozpadu resztek jedzenia. Dlatego zła higiena jamy ustnej często powoduje dziury w zębach, w których nadal znajdują się bakterie próchnicy. Na przykład, jeśli pasta do zębów zawiera fluor, następuje wymiana jonów hydroksylowych na jony fluorkowe. Tworzy to fluorapatyt, który okazuje się być twardszym materiałem i mniej wrażliwym na kwasy. Nawet hydroksyapatyt rozpuszczony w kwasach może ponownie wytrącić się jako fluoroapatyt w obecności fluorków.
W ten sposób można odwrócić początkowe zniszczenie. Ale fluorki mają również pozytywne właściwości w budowaniu kości. Tutaj spożycie odbywa się doustnie. Dzieciom i niemowlętom podaje się fluor i witaminę D, aby zapobiec krzywicy. Nie należy jednak przedawkować fluoru, aby nie doszło do rozwoju fluorozy ze sztywnością i zgrubieniem stawów. Związki fluoru są również zatwierdzone jako leki na osteoporozę. Odpowiednie tabletki zawierają fluorek sodu lub fluorofosforan disodu.
Edukacja, występowanie, właściwości i optymalne wartości
Fluor zawarty jest w postaci fluorków w czarnej i zielonej herbacie, szparagach, a także w rybach. Wiele soli zawiera fluor. Nie ma czystych soli fluoru ze względu na niską rozpuszczalność związków zawierających fluorki w wodzie. Fluorspar (fluorek wapnia) i fluorapatyt występują najczęściej w skorupie ziemskiej.
Fluor jest wytwarzany głównie z fluorku wapnia. Istnieją nawet organizmy, które mogą wytwarzać związki fluoroorganiczne. Południowoafrykańskie Gifblaar lub rośliny z rodzaju Dichapetalum mogą syntetyzować kwas fluorooctowy przeciwko drapieżnikom. Organizm ludzki potrzebuje dziennie 0,25-0,35 mg.
Choroby i zaburzenia
Jednak zatrucia związane z fluorem i problemy zdrowotne są bardziej powszechne. Jak wspomniano wcześniej, czysty fluor jest bardzo trującym gazem korozyjnym. To także utrudnia wytwarzanie fluoru.
Ponieważ reaguje z prawie wszystkimi materiałami, może być również bardzo słabo przechowywany i transportowany. Zatrucie fluorem powoduje oparzenia chemiczne i oparzenia płuc, skóry i oczu. W zależności od dawki odpowiednie narządy rozpuszczają się w krótkim czasie, powodując śmierć. Dawka śmiertelna jest bardzo niska i wynosi 185 ppm. Rzadko występuje zatrucie fluorem czystym fluorem, ponieważ gaz nie jest stabilny. Jednak zatrucie fluorowodorem jest podobnie niebezpieczne. Fluorowodór tworzy wiązania wodorowe z białkami organizmu, w wyniku czego trzeciorzędowa struktura białek ulega zniszczeniu. Następuje denaturacja białka organizmu.
Fluorki mogą tworzyć złożone związki z jonami glinu, które mają podobny efekt do fosforanów. W organizmie związki te wpływają na reakcje fosforylacji. Prowadzi to między innymi do deregulacji białek G, w wyniku czego wiele enzymów jest hamowanych. Tylko z tego powodu zwiększona dawka fluoru nie jest tolerowana przez organizm. Przyjmowanie zbyt dużej ilości tabletek z fluorem może również prowadzić do nudności, wymiotów i biegunki. Fluorek reaguje z kwasem żołądkowym, w wyniku czego powstaje niewielka ilość kwasu fluorowodorowego. To atakuje błony śluzowe. Przewlekłe, łagodne przedawkowanie fluoru może prowadzić do fluorozy.
Fluoroza to przewlekłe zatrucie fluorem ze zmianami w strukturze szkliwa zębów, kaszlem, plwociną i dusznością. Za dużo hydroksyapatytu zamienia się w zębach we fluoroapatyt. Zęby stają się bardziej kruche. Kości również się zmieniają z powodu nadmiernego tworzenia się fluorapatytu. Kości powoli sztywnieją i przebudowują się. Ponadto enzym enolaza jest hamowany.


.jpg)
.jpg)


.jpg)
.jpg)