Apicomplexa, również Sporozoa nazywane są jednokomórkowymi pasożytami z jądrem komórkowym, których rozmnażanie następuje naprzemiennie między schizogonią bezpłciową a sporozoitami wynikającymi z fuzji płciowej gamet. Z reguły zmiana jest związana ze zmianą hosta typową dla Apicomplexa. Najbardziej znanymi przedstawicielami apikompleksu, które należą do eukariotów, są plazmodia (patogen malarii) i Toxoplasma gondii (patogen toksoplazmozy).
Co to są kompleksy?
Apicomplexa to jednokomórkowe pasożyty z jądrem, dlatego zalicza się je do eukariontów. Swoją nazwę zawdzięczają tak zwanemu kompleksowi wierzchołkowemu, który jest wspólny dla wszystkich apikompleksów i który umożliwia pasożytom przebijanie błon komórkowych w celu umożliwienia ich tak zwanym roptriom, drobnym organellom komórkowym, przeniesienie ich enzymów litycznych i niektórych kinaz do cytoplazmy zaatakowanej komórki. Pusta komórka.
Apikompleksy są zasilane przez mikropory w ich złożonej błonie otaczającej, a nie przez fagocytozę. Chociaż apikompleksy utraciły rzęski i wici w toku ewolucji, mogą z łatwością meandrować i ślizgać się.
Cechą charakterystyczną Apicomplexa jest zmiana ich gospodarza, co zwykle wiąże się ze zmianą reprodukcji bezpłciowej na płciową. U niektórych gatunków zmiana żywiciela nie jest zbyt spektakularna i zachodzi od kręgowca do kręgowca. Cztery różne typy plazmodii, czynniki wywołujące malarię, przechodzą spektakularną zmianę żywiciela między komarem Anopheles a człowiekiem.
W rozmnażaniu bezpłciowym podział jąder i kolejne podziały komórkowe prowadzą do powstania do 4 merozoitów z każdej komórki, z których niektóre dalej rozwijają się w męskie mikrogamety i żeńskie makrogamety. Dwie gamety łączą się po zmianie żywiciela, a po mejozie i dalszych mitozach tworzą dużą liczbę zakaźnych sporozoitów, które rosną w oocystach.
Występowanie, rozmieszczenie i właściwości
Jest bardzo prawdopodobne, że Apicomplexa rozwinęła się w trakcie ewolucji w obowiązkowe pasożyty wewnątrz- lub zewnątrzkomórkowe. Ewolucja doprowadziła do utraty pierwotnie istniejących rzęsek lub wici, których nie potrzebują już pilnie w swoim obecnym stylu życia, ponieważ nie muszą już wachlować się jedzeniem, a potrzeba aktywnego poruszania się jest w dużej mierze wyeliminowana. Plasmodia żyjące wewnątrzkomórkowo w erytrocytach są dosłownie otoczone przez liczne składniki odżywcze w cytoplazmie, które muszą wchłonąć jedynie przez mikropory ich błony komórkowej.
Większość przedstawicieli Apicomplexa żyje zewnątrzkomórkowo w jamach ciała swoich gospodarzy. Zwykle jest to przewód pokarmowy. Zakaźne sporozoity, które wyznaczają początek cyklu infekcyjnego i rozwojowego, są wydalane z kałem i mogą nawet przetrwać „fazę oczekiwania” do dwóch lat w glebie w stanie nienaruszonym. Sporozoity z Apicomplexa są zatem wszechobecne w prawie wszystkich strefach klimatycznych.
Trochę inaczej wygląda to z plazmodiami, które żyją wewnątrzkomórkowo w erytrocytach. Są one zależne od zmiany żywiciela z komara Anopheles na ludzi lub inne kręgowce, tak więc, z kilkoma wyjątkami klinicznymi, zakażenie może nastąpić tylko przez trąbkę zakażonego komara. W ślinie komara znajdują się sporozoity, które przyczepiają się do tkanki wątroby i tam się namnażają. Później wracają do krwi i migrują do erytrocytów, gdzie rozwijają się dalej w zależności od rodzaju plazmodii. Niektóre z powstałych merozoitów dalej różnicują się w męskie mikrogamety i samice makrogamety, które mogą być spożywane przez samicę komara Anopheles i które ponownie rozwijają zakaźne sporozoity u komara w procesie rozmnażania płciowego w oocystach. Infekcja ogranicza się zatem do regionów, w których żyje Anopheles. Wyjątkiem są lotniska i porty, w których importowane zarażone komary Anopheles mogą przenosić malarię przez krótki czas.
Najważniejszymi apikompleksami są kokcydia, Toxoplasma gondii i opisane powyżej plazmodia. Wewnątrzkomórkowe kokcydia kolonizują głównie przewód pokarmowy wielu kręgowców i powodują kokcydiozę, zwykle łagodną z biegunką i podobnymi objawami. Toxoplasma gondii, czynnik wywołujący toksoplazmozę, żyje wewnątrzkomórkowo i preferuje komórki nabłonka jelitowego. Jedną z głównych dróg zakażenia są koty domowe, które są zakażane na przykład przez myszy i mogą również zarazić ludzi, jeśli wejdą w bliski kontakt.
Tutaj znajdziesz swoje leki
➔ Leki wzmacniające obronę i układ odpornościowyChoroby i dolegliwości
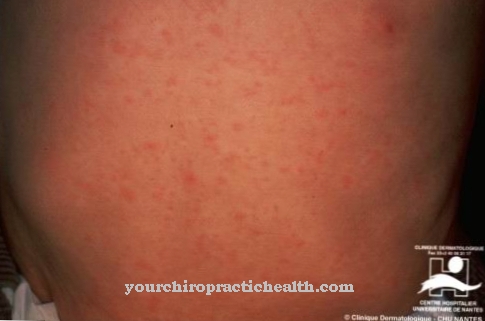
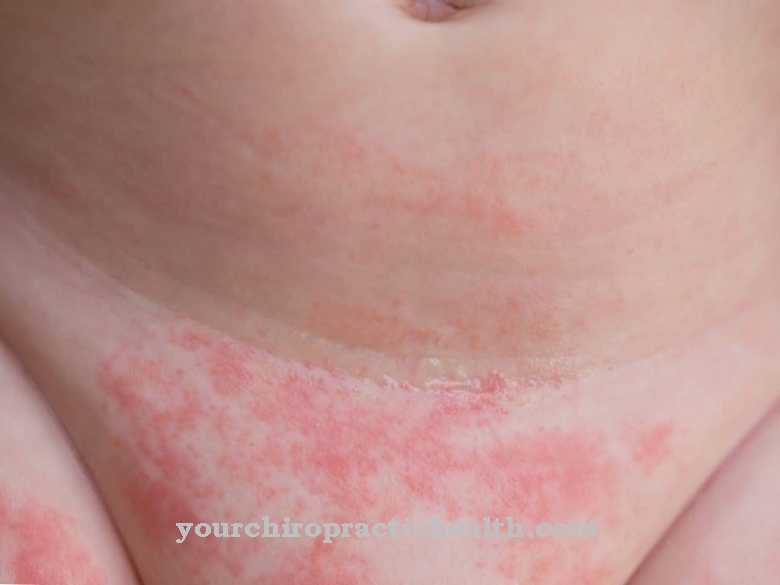
Cyklospory, izospory i kryptospory są szczególnie istotne jako przyczyna zakażeń kokcydiami u ludzi.Osoby z osłabionym układem odpornościowym są szczególnie narażone na zwiększone ryzyko infekcji. Kokcydioza objawia się niespecyficznymi objawami, takimi jak ciężka biegunka i skurcze brzucha, które - jeśli nie są leczone - mogą utrzymywać się przez kilka tygodni i prowadzić do poważnej utraty elektrolitów.
Toxoplasma gondii, przyczyna toksoplazmozy, często zakaża koty, które mogą przenosić zakaźne sporozoity na ludzi, jeśli wejdą w bliski kontakt z ludźmi. Jeśli patogen napotka nienaruszony układ odpornościowy, wydaje się, że nie ma żadnego niebezpieczeństwa, ponieważ występuje tylko kilka objawów związanych z chorobą lub nie występują wcale.
Zakaźne sporozoity mogą atakować komórki układu fagocytarnego i tworzyć tam komórki macierzyste poprzez tak zwaną endodyogenezę, z których każda ma dwie komórki potomne, które jako bradyzoity (również cystozoity) mogą bezobjawowo stać się we wszystkich narządach, w płynie, a nawet w OUN w tak zwanych pseudocystach. Chociaż torbiele rzekome są tłumione przez układ odpornościowy, mogą - nawet po kilku latach - wywołać rodzaj endogennej infekcji w osłabionym układzie odpornościowym, w wyniku ciąży, choroby lub sztucznej immunosupresji, bez ponownego kontaktu z patogenami.



.jpg)
.jpg)