Na Ścieżka ratunkowa nowa biocząsteczka jest syntetyzowana z produktów degradacji biocząsteczki. Ścieżka ratunkowa jest również znana jako ścieżka regeneracji i jest, by tak rzec, formą recyklingu w ramach metabolizmu.
Jaka jest ścieżka ratunkowa?
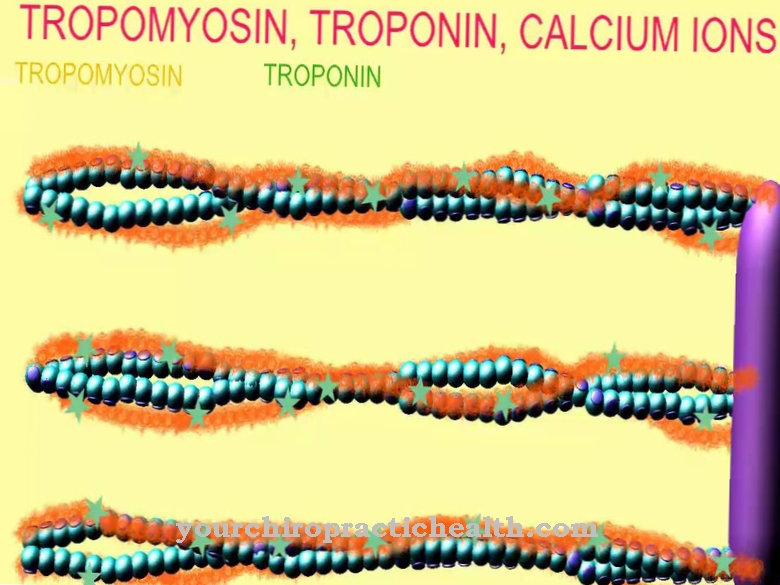
Ścieżka ratunkowa oznacza z jednej strony ogólną formę tego recyklingu w ramach metabolizmu, az drugiej strony szlak metaboliczny nukleotydów purynowych. Nukleotydy purynowe są podstawowym chemicznym budulcem kwasu dezoksyrybonukleinowego (DNA) i kwasu rybonukleinowego (RNA).
W odzyskiwaniu nukleotydów putinowych mononukleotydy powstają z zasad purynowych, guaniny, adeniny i hipoksantyny. W 90% ten szlak metaboliczny jest głównym szlakiem metabolicznym wolnych puryn. Reszta jest rozkładana na kwas moczowy. Szlak ratunkowy ma wiele zalet, zwłaszcza w porównaniu z biosyntezą de novo mononukleotydów purynowych. Na przykład jest znacznie bardziej energooszczędny.
Anatomia i budowa
Synteza bicyklicznych zasad purynowych wiąże się z dużym wysiłkiem organizmu. Dlatego są dzielone na proste bazy, a następnie używane ponownie.
Na ścieżce recyklingu różne produkty pośrednie rozpadu mononukleotydów, nukleozydów, polinukleotydów lub zasad kwasów nukleinowych są wykorzystywane do tworzenia reakcji zamiast ich całkowitego rozbicia. Dzięki reakcji na szlaku ratunkowym, użyteczne i cenne produkty pośrednie metabolizmu, tak zwane metabolity, można uratować przed utylizacją. Zatem te metabolity nie muszą być ponownie produkowane. Ten proces oszczędza wysokie zużycie energii przez ogniwo. W szlaku ratunkowym fosforan rybozy z pirofosforanu fosforybozylu (PRPP) jest przenoszony do wolnej zasady purynowej.
Nukleotyd powstaje przez odszczepienie pirofosforanu. Wymagane do tego enzymy są aktywowane przez pirofosforan fosforybozylu i hamowane przez produkty końcowe. Z adeniny w postaci zasady purynowej powstaje monofosforan adenozyny (AMP) razem z (PRPP) i za pomocą enzymu transferazy adeninofosforybozylowej (APRT). W połączeniu z PRPP i enzymem fosforybozylotransferazy hipoksantyno-guaninowej (HGPRT), guanina staje się nukleotydem monofosforanem guanozyny (GMP). Dzięki PRPP i enzymowi fosforybozylotransferazy hipoksantyno-guaninowej hipoksantyna staje się nukleotydem monofosforanem inozyny (IMP).
Inne enzymy zaangażowane w szlak ratunkowy to fosforylazy nukleozydowe, kinazy nukleozydowe i kinazy nukleotydowe. 90% puryn jest najpierw przekształcanych w nukleotydy, a następnie ponownie wykorzystywane do syntezy kwasów nukleinowych poprzez konwersje. 10% puryn jest rozkładanych na kwas moczowy i wydalanych przez nerki.
Funkcja i zadania
Szlak ratunkowy zachodzi w prawie wszystkich komórkach ciała, ponieważ puryny są rozkładane w prawie wszystkich komórkach ciała. Puryny należą do grupy heterocykli i obok pirymidyn są najważniejszymi budulcami kwasów nukleinowych. Puryny powstają przy użyciu samego szlaku ratunkowego. Są zawarte we wszystkich komórkach, które mają jądro.
Żywność pochodzenia zwierzęcego, zwłaszcza podroby i skóry, zawiera dużo puryn. Puryny, które nie są poddawane recyklingowi, są rozkładane na kwas moczowy i wydalane przez nerki. Nie ma wartości krwi dla szlaku ratunkowego, ale są dane dla kwasu moczowego. U mężczyzn stężenie kwasu moczowego we krwi wynosi zwykle od 3,4 do 7,0 mg / 100 ml. U kobiet liczba kwasu moczowego powinna wynosić od 2,4 do 5,7 mg / l.
Choroby
Jeśli istnieje wada na ścieżce ratunkowej, puryn nie można już poddać recyklingowi. Rozpada się znacznie więcej puryn, przez co powstaje więcej kwasu moczowego. Nerki nie są już w stanie całkowicie wydalać kwasu moczowego, co prowadzi do hiperurykemii.
Hiperurykemia to wzrost poziomu kwasu moczowego we krwi. Z definicji hiperurykemia występuje od poziomu kwasu moczowego 6,5 mg / dl. Wartość graniczna dotyczy jednakowo obu płci. Wzrost poziomu kwasu moczowego spowodowany przerwaniem szlaku ratunkowego jest również znany jako pierwotna hiperurykemia. Około 1% wszystkich przypadków hiperurykemii jest spowodowanych nadprodukcją kwasu moczowego w wyniku zaburzeń metabolizmu puryn. Większość pierwotnej hiperurykemii jest spowodowana zmniejszonym wydalaniem kwasu moczowego przez nerki.
Aby rozróżnić, czy zwiększone wartości moczu wynikają ze zmniejszonego wydalania, czy ze zwiększonej produkcji kwasu moczowego, należy określić klirens kwasu moczowego. Aby obliczyć klirens kwasu moczowego, oznacza się wydalanie kwasu moczowego w dobowej zbiórce moczu oraz stężenie kwasu moczowego w surowicy.
W większości przypadków hiperurykemia pozostaje bezobjawowa. W przypadku masywnej hiperurykemii dochodzi do ostrego ataku dny. W tym miejscu w stawach osadzają się skrystalizowane sole kwasu moczowego. Prowadzi to do zapalenia zajętych stawów z przegrzaniem, bólem i silnym zaczerwienieniem. Szczególnie często dotyczy to stawu śródstopno-paliczkowego, stawu skokowego i stawu kolanowego. Jeśli dna utrzymuje się przez długi czas, tkanka ulega przebudowie. Chrząstka w stawach pogrubia się i rozwija się tzw. Dna moczanowa.
Defektem genetycznym prowadzącym do hiperurykemii jest zespół Lescha-Nyhana. Choroba jest dziedziczona w sposób recesywny sprzężony z chromosomem X i skutkuje niedoborem enzymu fosforybozylotransferazy hipoksantyno-guaninowej (HGPRT). Ponieważ enzym bierze udział w metabolizmie puryn hipoksantyny i guaniny zasad purynowych, więcej puryn jest wytwarzanych do degradacji. Rezultatem jest gwałtowny wzrost poziomu kwasu moczowego. Choroba jest dziedziczona w sposób sprzężony z chromosomem X. Dlatego prawie wyłącznie mężczyźni są dotknięci zespołem Lescha-Nyhana. Pierwsze objawy pojawiają się około dziesięciu miesięcy po porodzie.
Dzieci przejawiają wyraźną postawę w połączeniu z siedzącym trybem życia i deficytami rozwojowymi. Pierwszym objawem jest często zwiększona ilość moczu w pieluszce. W ciężkich przypadkach mogą również wystąpić samookaleczenia, takie jak ugryzienia warg i palców oraz zaburzenia myślenia. Dzieci dotknięte chorobą mogą również zachowywać się agresywnie w stosunku do swoich rodziców, rodzeństwa, przyjaciół lub opiekunów.




.jpg)