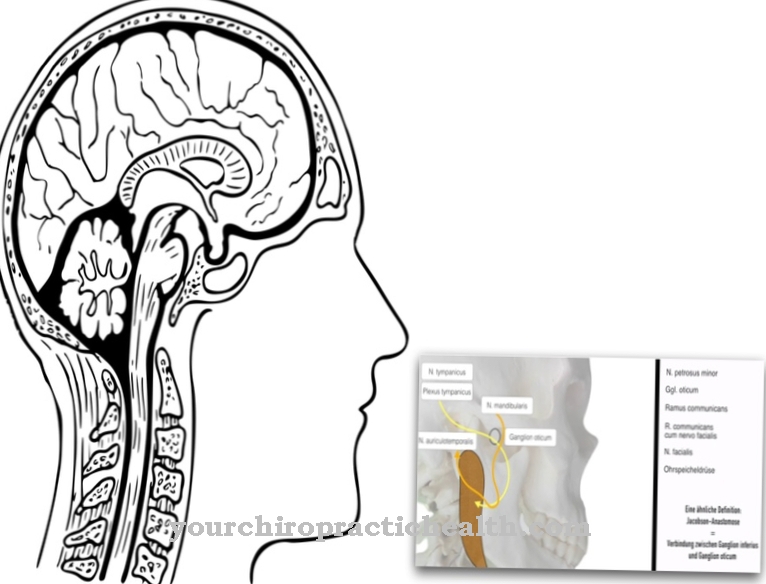
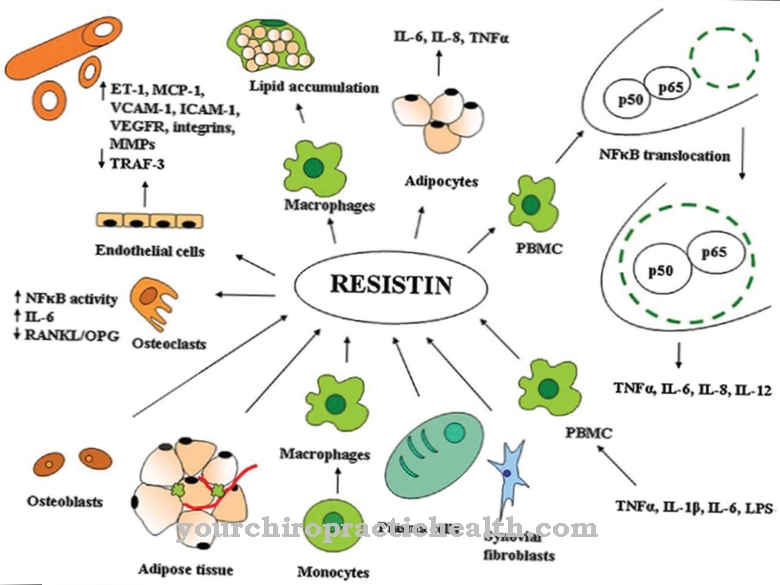
Lizosomy to organelle w komórkach organizmów żywych z rozwiniętymi jądrami komórkowymi (eukarionty). Lizosomy to pęcherzyki komórki otoczone błoną, zawierające enzymy trawienne. Zadaniem lizosomów utrzymywanych w środowisku kwaśnym jest rozkładanie substancji endogennych i egzogennych oraz w razie potrzeby inicjowanie destrukcji komórek (apoptozy).
Co to jest lizosom?
Lizosomy to pęcherzyki, czyli małe inkluzje komórkowe w komórkach eukariotycznych, które są otoczone błoną i zawierają wewnątrz różne wewnątrzkomórkowe, hydrolityczne enzymy trawienne. Są to proteazy, nukleazy i lipazy, czyli enzymy trawienne, które mogą rozkładać i rozkładać białka, kwasy nukleinowe i tłuszcze.
Fragmenty są dalej rozkładane i częściowo usuwane lub ponownie wykorzystywane przez metabolizm, że tak powiem, poddawane recyklingowi. Dlatego lizosomy są również określane jako własny żołądek komórki. Wnętrze lizosomów o średnicy od 0,1 do 1,1 mikrometra jest utrzymywane w środowisku kwaśnym o pH od 4,5 do 5,0 dzięki działaniu pomp protonowych. Silnie kwaśne środowisko służy do ochrony samej komórki, ponieważ enzymy są aktywne tylko w kwaśnym środowisku.
Jeśli lizosom opróżni swoje enzymy do cytozolu o neutralnym pH, są one natychmiast dezaktywowane i nieszkodliwe dla komórki. Aby sama membrana nie była atakowana przez enzymy trawienne, białka błonowe są silnie glikozylowane wewnątrz.
Funkcja, efekt i zadania
Głównym zadaniem lizosomów jest dostarczanie hydrolitycznych enzymów trawiennych, które w razie potrzeby rozkładają białka, kwasy nukleinowe i tłuszcze. Mogą to być substancje obce dla komórki lub ich własne. Rozpad substancji komórkowych obejmuje również apoptozę, zaprogramowaną wcześniej śmierć komórki, w której lizosomy wraz z enzymami przejmują zasadniczą funkcję techniczną.
Cząsteczki niekomórkowe, które znajdują się w przestrzeni zewnątrzkomórkowej i są przeznaczone do degradacji, są najpierw transportowane do komórki przez endocytozę. Zewnętrzna błona komórkowa odwraca się na lewą stronę, opływa substancję, która ma zostać rozbita, a następnie oddziela się od błony komórkowej jako niezależny pęcherzyk. Pęcherzyki łączą się z lizosomami, dzięki czemu może rozpocząć się proces rozpadu. Proces endocytozy i fuzji z lizosomem przebiega zawsze bez bezpośredniego kontaktu z cytoplazmą i jest porównywalny z fagocytozą.
W ramach niezależnego procesu odnowy komórkowej do lizosomów doprowadzane są również inne organelle i składniki cytozolu w celu „rozkładu”. Z reguły fragmenty są ponownie wykorzystywane do odbudowy aminokwasów, białek, kwasów nukleinowych i węglowodanów, czyli poddawane recyklingowi. Lizosomy odgrywają również ważną rolę w apoptozie, programowanej śmierci komórki. Komórka, która otrzymała sygnał apoptozy, jest kurczona i rozkładana zgodnie z określonym programem, bez przedostawania się części komórki do przestrzeni zewnątrzkomórkowej, gdzie reakcje zapalne miałyby miejsce natychmiast.
Edukacja, występowanie, właściwości i optymalne wartości
Praktycznie, z nielicznymi wyjątkami, lizosomy występują w każdej komórce eukariontów. Jedynie liczba lizosomów przypadających na komórkę zmienia się w zależności od typu komórki i zadań komórki w tkance. Enzymy hydrolityczne i białka błony lizosomu są syntetyzowane przez rybosomy w siateczce endoplazmatycznej (ER). Następnie są znakowane w aparacie trans-Golgiego, aby nie były przypadkowo przenoszone do żadnych lizosomów.
Najważniejszą rolę w znakowaniu odgrywa fosfotransferaza i inny enzym, który dopełnia proces znakowania. Kwaśne środowisko w lizosomach zapewnia ATPaza typu V. Enzym oddziela 2 jony H + z ATP w procesie hydrolizy i transportuje je do lizosomu. Lizosomy biorą udział w wielu wewnętrznych i zewnętrznych procesach metabolicznych. Bezpośredni lub pośredni pomiar ich liczby nie jest możliwy i miałby niewielką wartość informacyjną. Dlatego nie można sformułować żadnej opinii na temat optymalnej liczby lizosomów. Wszelkie awarie w lizosomach są zwykle bardzo zauważalne.
Choroby i zaburzenia
Istnieje kilka znanych dysfunkcji lizosomów, które prowadzą do poważnych chorób. Bardzo rzadko występujące - genetyczne - zaburzenie czynnościowe jest wywołane defektem fosfotransferazy. Nieoperacyjny enzym prowadzi do niekontrolowanego uwalniania enzymów lizosomalnych do macierzy zewnątrzkomórkowej.
Jednocześnie dochodzi do kumulacji lipidów, mukopolisacharydów i glikoprotein w lizosomach, które w rzeczywistości są przeznaczone do degradacji i degradacji. Ale ponieważ nie ma enzymów trawiennych z powodu ich niewłaściwego kierunku, substancje te gromadzą się coraz bardziej w lizosomach. Ta autosomalna, recesywna dziedziczna lizosomalna choroba spichrzeniowa, znana jako choroba komórek I, jest oparta na mutacji w genie GNPTAB. Znane są inne lizosomalne choroby spichrzeniowe, ale są one oparte na nieprawidłowo zsyntetyzowanych hydrolazach. Podobnie jak w przypadku choroby I-komórek, również tutaj dochodzi do nagromadzenia niezdegradowanych białek, kwasów nukleinowych i lipidów.
Cechą wspólną wszystkich lizosomalnych chorób spichrzeniowych jest to, że proporcja substancji wprowadzanych do substancji uwalnianych z lizosomów jest zaburzona kosztem substancji, które mają być uwalniane. W lizosomach występuje prawdziwe zatory. Choroby spichrzowe zwykle mają poważny przebieg i nie można ich wyleczyć pod względem usunięcia przyczyny.
Inne ryzyko pojawia się podczas przyjmowania leków lipofilnych o słabej zasadzie. Mogą przechodzić przez błony lizosomów w postaci obojętnej z zewnątrz do wewnątrz, ale nie w przeciwnym kierunku, jeśli są protonowane przez kwaśne środowisko w lizosomach, tak że może wystąpić lizosomotropia, czyli nagromadzenie leków w lizosomach. .Substancje lecznicze w lizosomach mogą osiągnąć stężenie od 100 do 1000 razy większe niż stężenie w osoczu krwi.


.jpg)

-durch-vitamin-b12-mangel.jpg)