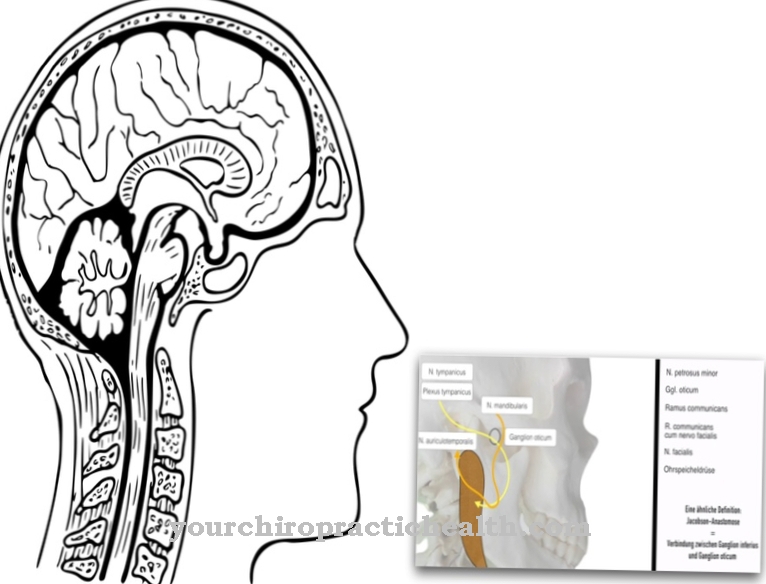
Tak jak Homocystynuria jest rzadką, uwarunkowaną genetycznie chorobą metaboliczną, której przyczyną jest niedobór enzymu i która charakteryzuje się zwiększonym stężeniem homocysteiny we krwi. Homocystynurię można zwykle dobrze leczyć za pomocą wczesnej i konsekwentnej terapii.
Co to jest homocystynuria?

© Anastasia Okhrimenko - stock.adobe.com
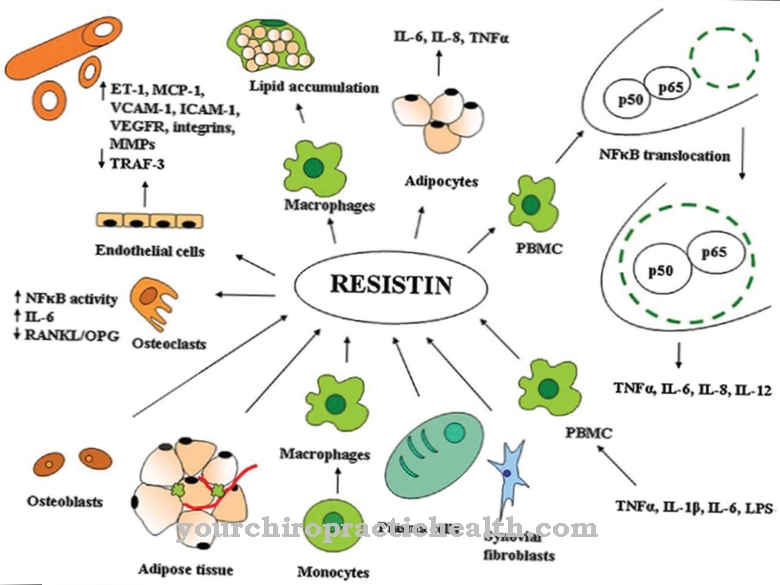
Tak jak Homocystynuria jest rzadką, genetycznie uwarunkowaną chorobą metabolizmu aminokwasów, spowodowaną defektami różnych enzymów biorących udział w metabolizmie metioniny (aminokwas egzogenny).
Homocysteina i homocystyna są produktami degradacji lub pośrednimi tego procesu metabolicznego i są natychmiast dalej metabolizowane u zdrowych ludzi. Ze względu na obecność wadliwych enzymów jest to możliwe tylko w ograniczonym stopniu u osób dotkniętych homocystynurią, tak że zwiększa się stężenie homocysteiny we krwi i homocystyny w moczu.
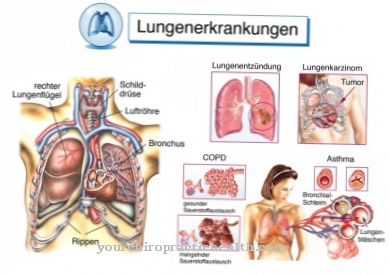
Zwiększone stężenie tych aminokwasów, które są uważane za toksyczne, może uszkodzić różne układy narządów. Choroby oczu (zwichnięcie soczewki, krótkowzroczność, jaskra), zmiany szkieletowe (osteoporoza, marfanoidalne długie kończyny), uszkodzenie ośrodkowego układu nerwowego (upośledzenie umysłowe i fizyczne, skurcze, zaburzenia naczyniowo-mózgowe) i układu naczyniowego (zatorowość, niedrożność naczyń) są charakterystycznymi następstwami homocystynurii.
przyczyny
Homocystynuria Wynika to z autosomalnego recesywnego dziedziczonego defektu genetycznego, który skutkuje niedoborem różnych enzymów biorących udział w metabolizmie metioniny. W zależności od enzymu i podprocesu metabolizmu metioniny, na który ma on wpływ, rozróżnia się trzy formy homocystynurii.
Im częściej Typ I. W homocystynurii występuje niedobór enzymu beta-syntazy cystationu (CBS), który zaburza syntezę cysteiny z metioniny. W rezultacie homocysteina gromadzi się we krwi (hiperhomocysteinemia), a homocystyna w moczu (homocystynuria).
Typ II Homocystynuria charakteryzuje się brakiem reduktazy 5,10-metylenotetrahydrofolianu (MTHFR), która reguluje syntezę metioniny z homocysteiny. Ten podproces metaboliczny jest odpowiednio zaburzony u osób cierpiących na typ II i oprócz wzbogacenia surowicy w homocysteinę może również prowadzić do niedoboru metioniny.
Typ III homocystynuria charakteryzuje się niedoborem kobalaminy (koenzym witaminy B12). Kobalamina bierze również udział w syntezie metioniny z homocysteiny, więc niedobór może również powodować zwiększone stężenie homocysteiny we krwi i niedobór metioniny.
Objawy, dolegliwości i oznaki
Homocystynuria może występować w różnych formach. Objawy są zróżnicowane i różnią się w zależności od etapu życia. Przed ukończeniem drugiego roku życia objawy choroby pojawiają się tylko w szczególnie rzadkich przypadkach. Oprócz charakterystycznych wyników laboratoryjnych noworodki z homocystynurią są normalne.
Zazwyczaj poziom homocysteiny we krwi jest znacznie podwyższony. Uszkadza to naczynia krwionośne, co w dłuższej perspektywie może prowadzić do zwapnienia naczyń (arteriosklerozy) i związanej z tym zatorowości i zakrzepicy. W rezultacie oczekiwana długość życia osób dotkniętych chorobą jest znacznie ograniczona. Najbardziej zauważalnym objawem zaburzeń metabolicznych wieku dziecięcego jest wypadnięcie soczewki oka.
Często wiąże się to z krótkowzrocznością. Im wcześniej pojawią się pierwsze oznaki choroby, tym większe ryzyko wystąpienia upośledzenia psychoruchowego (niepełnosprawności intelektualnej), które jest nieodwracalne. Większość osób dotkniętych chorobą ma osteoporozę już w dzieciństwie. W rezultacie kręgosłup spłaszcza się i stopniowo deformuje.
Wysoki poziom homocysteiny często prowadzi do wysokiego wzrostu i objawów, które mogą być podobne do zespołu Marfana. Należą do nich obecność piersi kurczaka i lejka, przemieszczona soczewka oka (zwichnięcie soczewki lub ektopia soczewki), jaskra (jaskra), odwarstwienie siatkówki i palce pająka (arachnodaktylia).
Diagnoza i przebieg
Aby zdiagnozować Homocystynuria stosowane są różne analizy laboratoryjne. Jeśli analiza moczu (np. Próba cyjankowo-nitroprusydkowa) wykaże podwyższone stężenie homocystyny i / lub obniżone stężenie metioniny (typ II i III), może to wskazywać na homocystynurię.
Analiza krwi może służyć do określenia stężenia homocysteiny w surowicy i zdiagnozowania hiperhomocysteinemii związanej z homocystynurią. Diagnoza jest potwierdzana przez hodowlę komórek z tkanki łącznej lub próbki tkanki wątroby, dzięki czemu można bezpośrednio wykryć podstawowy defekt genetyczny.
Przebieg homocystynurii może być różny u różnych osób pod względem objawów i chorób wtórnych. Przy wczesnym rozpoznaniu i wczesnym rozpoczęciu leczenia homocystynuria ma zwykle korzystny przebieg i dobre rokowanie.
Komplikacje
Homocystynuria prowadzi przede wszystkim do poważnych dolegliwości psychologicznych, które mogą mieć wyjątkowo negatywny wpływ na życie pacjenta i życie codzienne. W większości przypadków dochodzi do silnego zaburzenia osobowości, któremu towarzyszą zaburzenia zachowania. Te zaburzenia mogą prowadzić do poważnych powikłań, zwłaszcza u dzieci.
Zazwyczaj pacjent jest dotknięty wykluczeniem społecznym i coraz bardziej wycofuje się z życia. Nierzadko prowadzi to do nastrojów depresyjnych. Ponadto w oczach występują dolegliwości, które mogą na przykład powodować jaskrę lub krótkowzroczność. Różne choroby naczyń krwionośnych również występują znacznie wcześniej i mogą prowadzić do ograniczeń w ruchu.
Samo leczenie z reguły nie prowadzi do szczególnych powikłań i odbywa się za pomocą leków. Choroba rozwija się pozytywnie stosunkowo szybko. W większości przypadków nie ma dalszych objawów nawet po zabiegu. Wczesne leczenie nie skraca oczekiwanej długości życia. Dolegliwości psychologiczne mogą być leczone wspomagająco przez psychologa.
Kiedy powinieneś iść do lekarza?
Jeśli pojawią się objawy, takie jak zaburzenia zachowania, zakrzepica lub opóźnienia w rozwoju, zdecydowanie należy zgłosić się do lekarza. Na wczesnym etapie należy również wyjaśnić objawy osteoporozy lub miażdżycy. Lekarz musi ustalić przyczynę objawów i jeśli to konieczne, rozpocząć leczenie. Dlatego wymienione objawy należy szybko wyjaśnić. Osoby z defektem genetycznym są szczególnie podatne na rozwój homocystynurii. Osoby dotknięte chorobą powinny dokładnie skonsultować się z lekarzem rodzinnym i poinformować ich o wszelkich nietypowych objawach.
Zasadniczo należy wyjaśnić skargi, które utrzymują się dłużej niż kilka dni lub nasilają się przez dłuższy czas. Charakterystyczne objawy homocystynurii zwykle rozwijają się podstępnie i często są rozpoznawane dopiero wtedy, gdy pojawiły się już nieodwracalne choroby. Tym ważniejsze jest rozpoznanie wczesnych objawów i poddanie ich leczeniu. Osoby, które zauważą u siebie lub u innych fizyczne lub psychiczne zmiany, które mogą być związane z zaburzeniami metabolicznymi, powinny jak najszybciej porozmawiać z lekarzem rodzinnym. Pozostałymi kontaktami są specjaliści chorób wewnętrznych lub poradnia specjalistyczna chorób dziedzicznych.
Lekarze i terapeuci w Twojej okolicy
Leczenie i terapia
Terapia Homocystynuria zależy od rodzaju choroby lub defektu enzymatycznego i ma na celu zmniejszenie i wyeliminowanie zwiększonego stężenia toksycznej homocysteiny. Homocystynurię typu I leczy się pirydoksyną (witaminą B6), gdy występuje resztkowa aktywność wadliwego enzymu.
Substancja zwiększa aktywność enzymatyczną i obniża stężenie homocysteiny we krwi. Około 50 procent osób dotkniętych tym typem bardzo dobrze reaguje na terapię doustną dużymi dawkami witaminy B6. Ponadto w celu wspomagania terapii zaleca się dietę ubogą w metioninę i bogatą w cystynę.
W przypadku obecności resztkowej aktywności enzymatycznej w homocystynurii typu II i III, w której zaburzona jest synteza metioniny z homocysteiny, podejmuje się próby ograniczenia tego zaburzenia preparatami kobalaminowymi (witamina B12). W przypadku obu postaci homocystynurii wskazana jest dieta bogata w metioninę.
Dodatkowo w leczeniu typu II stosuje się kwas foliowy, który również wpływa pozytywnie na aktywność wadliwej reduktazy 5,10-metylenotetrahydrofolianu, a także metioninę i betainę. Leki przeciwzakrzepowe (kwas acetylosalicylowy) pomagają zapobiegać chorobom naczyniowym, takim jak zakrzepica i zator.
Perspektywy i prognozy
Przy wczesnej diagnostyce i intensywnej terapii rokowanie w przypadku homocystynurii jest zwykle korzystne. Choroba nie jest uleczalna, ponieważ jest defektem genetycznym. Jednak w ramach terapii istnieje możliwość trwałego obniżenia stężenia homocysteiny i metioniny, co znacznie zmniejsza prawdopodobieństwo wystąpienia zaburzeń i powikłań rozwojowych.
Stopień ciężkości homocystynurii może być różny. Istnieją formy choroby, które na początku są normalne, a poza tym są łagodne. Jednak nawet tutaj od 20 lub 30 roku życia istnieje większe ryzyko rozwoju miażdżycy, zakrzepicy, zatorowości, zawału serca i udaru mózgu.
Jeśli jednak stężenie homocysteiny jest już bardzo wysokie w okresie niemowlęcym, bez intensywnego leczenia istnieje duże ryzyko wystąpienia zaburzeń rozwoju fizycznego i psychicznego dziecka. Upośledzenie umysłowe może ujawnić się już w pierwszych dwóch latach życia. Dzieci dotknięte chorobą często cierpią również na osteoporozę. Aż 70 procent nieleczonych dzieci ma problemy ze wzrokiem, które najwyraźniej przejawiają się w wypadnięciu soczewki oka. Inne konsekwencje dla oczu to jaskra, skrajna krótkowzroczność, odwarstwienie siatkówki i ślepota. Jeśli ciężkie postacie choroby są leczone zbyt późno lub wcale, zakrzepica i zatorowość rozwiną się u 30 procent wszystkich pacjentów w wieku poniżej 20 lat.
zapobieganie
Tam Homocystynuria jest chorobą genetyczną, której nie można zapobiec. Jeśli jednak leczenie rozpocznie się wcześnie, powikłaniom homocystynurii można zapobiec lub je ograniczyć. Ponadto osoby dotknięte chorobą mają możliwość poddania nienarodzonego dziecka badaniu homocystynurii w ramach diagnostyki prenatalnej (analiza płynu owodniowego). Zaleca się również badanie rodzeństwa osób dotkniętych chorobą w kierunku homocystynurii.
Opieka postpenitencjarna
W zależności od rodzaju defektu enzymatycznego, który jest przyczyną zaburzeń metabolicznych, przydatny i niezbędny jest cały szereg środków w ramach kontynuacji leczenia homocystynurii. W przypadku homohystynurii typu I, oprócz medycznego podawania witaminy B6, pacjent musi przestrzegać diety bogatej w witaminy. Witamina B6 zwiększa aktywność wadliwego enzymu iw konsekwencji prowadzi do obniżenia stężenia homocysteiny we krwi.
Aby ten efekt został utrzymany, dieta musi być stale przestrzegana. To samo dotyczy spożywania pokarmów bogatych w cystynę i ubogich w metioninę. W przypadku homocystynurii typu II należy również kontynuować dietę, aby osiągnąć długotrwałe efekty. Ponadto podczas działań następczych przeprowadzane są regularne kontrole. Lekarz musi sprawdzić aktywność zaatakowanych enzymów iw razie potrzeby dostosować terapię.
Ponieważ homocystynuria zwykle nie jest poważną chorobą, wystarczające są badania lekarskie co trzy do sześciu miesięcy. W przypadku ciężkich zaburzeń należy konsultować się ze specjalistą co miesiąc po zakończeniu właściwej terapii. Ponadto należy zwrócić uwagę na nietypowe objawy, ponieważ zaburzenie metaboliczne może w dłuższej perspektywie powodować inne choroby, które należy leczyć.
Możesz to zrobić sam
W zależności od rodzaju defektu enzymatycznego leżącego u podstaw homocystynurii i stosowanej przez lekarza terapii, pacjent może sam zrobić kilka rzeczy, aby złagodzić objawy.
Przede wszystkim ważna jest dieta bogata w cystynę. Ofiara powinna spożywać głównie ryż, orzechy, soję i produkty owsiane. Składnik aktywny znajduje się również w arbuzach, nasionach słonecznika i zielonej herbacie. Lekarz przepisze również suplementy witaminy B12, aby ograniczyć upośledzenie. Osoba poszkodowana może wesprzeć te środki, tworząc wraz z dietetykiem plan diety bogatej w metion i konsekwentnie go wdrażając. Należy unikać pokarmów bogatych w białko, takich jak jajka lub mięso. Dozwolone są produkty niskobiałkowe, w tym owoce, warzywa i makaron niskobiałkowy, chleb lub mąka ze specjalistycznych sklepów. Ta dieta powinna być również wspomagana różnymi witaminami z grupy B i kwasem foliowym.
Po ustąpieniu choroby pacjent powinien przejść dodatkowe badania kontrolne. Homocystynuria jest chorobą trwającą całe życie, wymagającą regularnej oceny w specjalistycznym ośrodku leczniczym. Ścisła kontrola umożliwia identyfikację problemów metabolicznych i leczenie na wczesnym etapie, zanim pojawią się powikłania.

-eisenmangelanmie.jpg)
.jpg)





-durch-vitamin-b12-mangel.jpg)