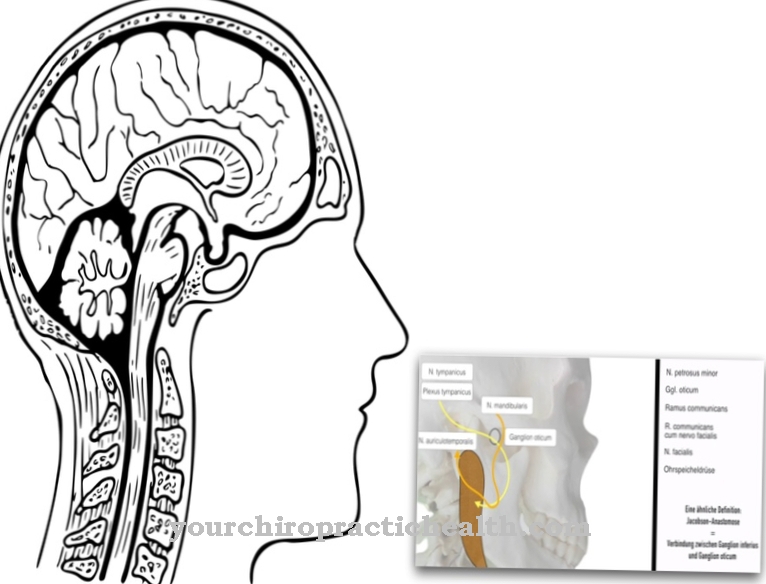
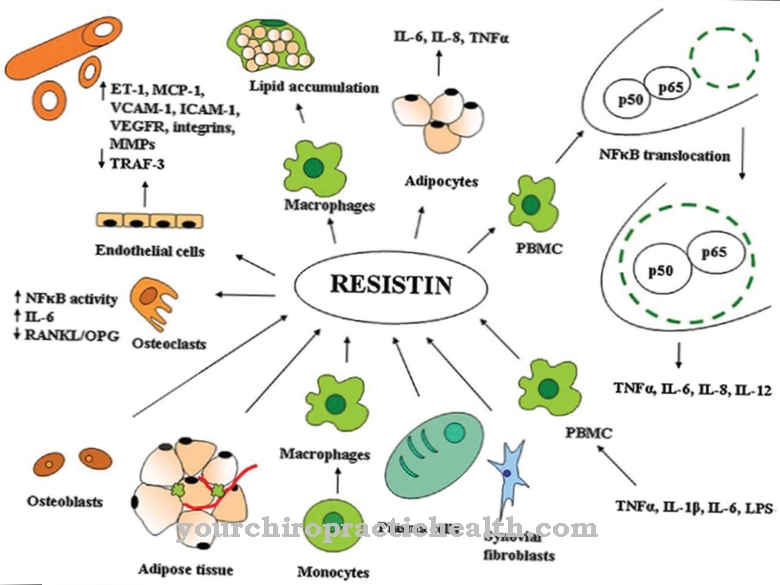
Fenyloalanina jest proteinogennym, niezbędnym aminokwasem z aromatycznym sześcioczłonowym pierścieniem, który działa jako budulec wielu białek i peptydów.
Ponadto fenyloalanina odgrywa ważną rolę w metabolizmie azotu i może być przekształcana w wątrobie w białkowy aminokwas tyrozynę. Fenyloalanina i tyrozyna odgrywają ważną rolę w syntezie insuliny, melaniny, tyroksyny oraz neuroprzekaźników dopaminy, serotoniny i tyraminy.
Co to jest fenyloalanina?
Fenyloalanina jest niezbędnym alfa-aminokwasem, który - w przeciwieństwie do większości aminokwasów proteinogennych - jest bioaktywny nie tylko w formie L, ale w ograniczonym stopniu również jako enancjomer w postaci R.
R-fenyloalanina jest w dużej mierze nieaktywna biochemicznie i występuje wyłącznie w sztucznym wytwarzaniu aminokwasu, ale dyskutowana jest rola D-fenyloalaniny w kontroli niektórych neuroprzekaźników w zespole bólu. Charakterystyczną cechą strukturalną fenyloalaniny jest prosty aromatyczny sześcioczłonowy pierścień (pierścień benzenowy) z dołączonym łańcuchem węglowodorowym. Chemiczny wzór strukturalny to C6H5-CH2-CH (NH2) -COOH, gdzie grupa C6H5 wskazuje na pierścień benzenowy. Aminokwas jest amfifilowy, co oznacza, że jest rozpuszczalny w tłuszczach i wodzie.
Wzór chemiczny pokazuje również, że fenyloalanina składa się wyłącznie z węgla, wodoru, azotu i tlenu, substancji, które są wszechobecne. Rzadkie metale, minerały lub pierwiastki śladowe nie są częścią aminokwasu. Niemniej jednak ludzki metabolizm nie może w wystarczającym stopniu syntetyzować fenyloalaniny z tyrozyny, ale jest zależny od spożycia z pożywienia. Fenyloalanina jest obecna w wystarczających ilościach w wielu produktach pochodzenia zwierzęcego i roślinnego, więc przy normalnej, mieszanej diecie - pod warunkiem, że przewód pokarmowy jest normalnie przyswajalny - nie ma potrzeby obawiać się niedoboru aminokwasu.
Funkcja, efekt i zadania
Najważniejszą funkcją i zadaniem fenyloalaniny jest udział w budowie wielu białek i peptydów. Bierze również udział w syntezie niektórych hormonów, które odgrywają kluczową rolę w kontroli procesów metabolicznych.
Istnieją hormony takie jak adrenalina, norepinefryna, L-dopa, PEA i melanina. Ponadto L-fenyloalanina służy jako substancja podstawowa, z której z. B. syntetyzowana jest substancja przekaźnikowa dopamina, serotonina, tyramina i inne. L-fenyloalanina służy również jako materiał wyjściowy dla niezbędnego aminokwasu tyrozyny. W tym celu fenyloalanina jest przekształcana w tyrozynę w wątrobie w dwóch etapach poprzez hydroksylację i rozszczepienie cząsteczki wody. Hydroksylaza fenyloalaninowa jest enzymem katalizującym przemianę do tyrozyny.
Alternatywne dostarczanie również niezbędnego aminokwasu tyrozyny - podobnie jak w przypadku fenyloalaniny - może odbywać się poprzez przyjmowanie pokarmu. W przeciwieństwie do wszystkich innych aminokwasów, które wykazują działanie bioaktywne tylko w swojej postaci L, enancjomer D fenyloalaniny wydaje się mieć przynajmniej wpływ na odczuwanie bólu. Stwierdzono, że mieszanina L- i D-fenyloalaniny (mieszanina racemiczna) ma działanie przeciwbólowe. Mieszanina DL prawdopodobnie blokuje rozkład enkefalin - własnych opioidów organizmu - dzięki czemu działanie przeciwbólowe jest przedłużone i zintensyfikowane.
Edukacja, występowanie, właściwości i optymalne wartości
Niezbędny aminokwas fenyloalanina jest wchłaniany z pożywieniem. Nie jest wolny, ale zwykle stanowi część białka lub polipeptydu w postaci związanej chemicznie. Aby aminokwas był dostępny do metabolizmu, odpowiednie białko musi najpierw zostać rozłożone w trakcie trawienia, a następnie ekstrahowane z „fragmentów” przy użyciu dalszych enzymów w dalszym metabolizmie.
L-fenyloalanina jest syntetyzowana tak zwaną drogą kwasu szikimowego. Jest to złożona biokatalityczna reakcja łańcuchowa, którą mają autotroficzne rośliny i bakterie. Cechą szczególną organizmów autotroficznych jest ich zdolność do tworzenia materii organicznej wyłącznie z materiału nieorganicznego. Wolna L-fenyloalanina ma gorzki smak, a jej enancjomer D, który jest wytwarzany wyłącznie w produkcji przemysłowej, ma słodkawy smak. Aminokwasem jest z. B. oferowany jako suplement diety i jest również częścią sztucznego słodzika aspartamu. Biodostępna L-fenyloalanina występuje w postaci związanej w wielu produktach spożywczych.
Ich zawartość jest szczególnie wysoka w suszonym groszku i soi, w orzechach włoskich i pestkach dyni, a także w różnych gatunkach ryb i mięs. Zapotrzebowanie na fenyloalaninę jest silnie uzależnione od podaży tyrozyny. Jeśli w diecie nie ma tyrozyny, organizm potrzebuje 38 do 52 mg na kg masy ciała. Przy bogatej podaży tyrozyny w diecie dzienne zapotrzebowanie spada do zaledwie 9 mg na kg masy ciała. Z reguły żywność zawierająca fenyloalaninę zawiera również odpowiednią ilość tyrozyny.
Zalecenie FAO / WHO z 1985 r. Sprowadza się do łącznego zapotrzebowania na L-fenyloalaninę i L-tyrozynę w ilości 14 mg na kg masy ciała dziennie. Dlatego osoba dorosła o masie ciała 80 kg potrzebuje 1120 mg obu substancji dziennie.
Choroby i zaburzenia
Objawy niedoboru przy trwale niewystarczającej podaży fenyloalaniny i tyrozyny w diecie są niezwykle rzadkie, ale mogą mieć poważne konsekwencje, szczególnie w obszarze neuronalnym.
Oprócz upośledzenia syntezy wielu hormonów i neuroprzekaźników na niedobór może wskazywać również zaburzenie mielinizacji włókien nerwowych. Przeciwieństwem niedoboru może być nadmierne stężenie fenyloalaniny (fenyloketonuria) z powodu genetycznego zaburzenia metabolicznego. Choroba jest dziedziczona autosomalnie recesywnie i prowadzi do zmniejszonej produkcji enzymu hydroksylazy fenyloalaniny, który może przekształcić fenyloalaninę w tyrozynę.
Zmniejszona aktywność enzymatyczna prowadzi do gwałtownego wzrostu aminokwasu, znanego jako fenyloketonuria, ponieważ przemiana do tyrozyny jest również drogą rozkładu fenyloalaniny. Jednocześnie brakuje tyrozyny, ponieważ droga syntezy jest zablokowana. Inną dziedziczną chorobą w tym kontekście jest zespół Hartnupa. Jest to zaburzenie metaboliczne, które zakłóca transport fenyloalaniny przez błonę komórkową. Prowadzi to do poważnych problemów w OUN, na skórze i przewodzie pokarmowym.




-durch-vitamin-b12-mangel.jpg)